不典型增生是人体细胞在长期慢性刺激下发生形态和功能异常的病理状态,它像一颗“定时”,可能发展为恶性肿瘤,也可能在干预下回归正常。这种介于健康与疾病之间的灰色地带,让无数人陷入焦虑——究竟哪些变化需要警惕?如何阻断癌变进程?
一、不典型增生的生物学本质:细胞失控的早期信号
在显微镜下,不典型增生的细胞呈现三大特征:核质比例失衡(细胞核异常增大)、极向紊乱(排列失去正常层次)、分裂异常(出现非典型核分裂象)。这些改变源于基因层面的驱动因素:
以胃黏膜为例,正常腺体呈规律性排列,细胞核位于基底部。当发生低级别不典型增生时,腺体开始拥挤变形,细胞核上移占据1/3胞质;进展到高级别时,核分裂象增多,腺体出现"背靠背"现象。
二、临床警示:这些症状可能提示癌变风险
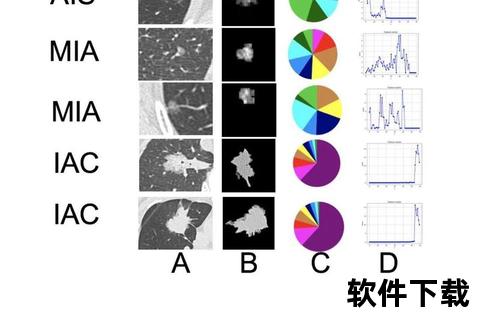
不典型增生本身通常无症状,但伴随的基础疾病会释放预警信号:
特殊人群需特别注意:
三、诊断金标准:分层管理的精准策略
1. 初筛手段
2. 病理分级系统(以宫颈病变为例)
| 分级 | 病变范围 | 癌变风险 | 管理策略 |
|||||
| CIN1 | 下1/3上皮 | <1% | 观察随访 |
| CIN2 | 下2/3 | 5-15% | 冷冻/LEEP |
| CIN3 | 全层 | >50% | 锥切手术 |
3. 分子诊断进展
四、干预策略:逆转癌变的时间窗口
1. 可逆阶段(低级别病变)
2. 临界阶段(高级别病变)
3. 术后管理黄金法则
五、预防体系:构筑三级防线
值得关注的是,表观遗传时钟研究显示,通过地中海饮食(橄榄油+深海鱼)、间歇性禁食(16:8模式),可使生物年龄逆转3-5年,从根本上降低病变风险。
当病理报告出现“不典型增生”,不必过度恐慌,但务必建立动态监测档案。记住两个关键时间节点:发现低级别病变的6个月内完成病因干预,高级别病变确诊后30天内决定治疗方案。现代医学已能精准拦截90%以上的癌变进程,真正决定结局的,是患者对规范化管理的执行力。
