新生儿黄疸是婴儿出生后最常见的代谢问题之一,超过60%的足月儿和80%的早产儿会出现皮肤、黏膜黄染的现象。这种看似普通的生理现象背后,实则隐藏着复杂的胆红素代谢机制与母婴健康因素的交互作用。本文将从科学角度解析其成因,并为家长提供实用的应对建议。
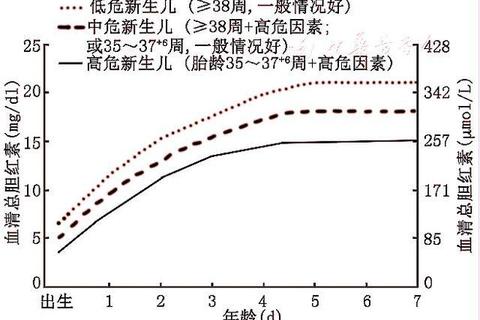
一、胆红素代谢异常的三大核心环节
新生儿黄疸的核心在于胆红素生成与代谢失衡。胆红素作为红细胞分解的产物,需经历以下代谢过程:
1. 生成阶段:新生儿红细胞寿命短(约90天),每天约1%的红细胞自然分解,产生未结合胆红素。母婴血型不合(如ABO或Rh溶血)会加速红细胞破坏,使胆红素生成量激增。

2. 肝脏处理阶段:婴儿肝脏的葡萄糖醛酸转移酶活性不足,导致未结合胆红素无法有效转化为水溶性结合胆红素。早产儿此酶活性仅为足月儿的30%,成为黄疸高发的重要原因。
3. 排泄阶段:结合胆红素需通过胆管排入肠道。先天性胆道闭锁、胆汁淤积等疾病会阻断排泄路径,导致黄疸迁延不愈。母乳中的β-葡萄糖醛酸苷酶也可能增加胆红素肠肝循环,延长黄疸时间。
二、母婴健康对黄疸的双重影响
(一)母亲因素
1. 妊娠期疾病:妊娠期糖尿病或高血压会改变胎盘功能,增加胎儿红细胞增多症风险,间接导致新生儿胆红素生成增加。
2. 感染与用药:孕期巨细胞病毒、弓形虫等感染可能损害胎儿肝功能;磺胺类、吲哚美辛等药物则会竞争胆红素结合位点。
(二)新生儿个体特征
1. 喂养方式:母乳喂养不足导致排便减少,胆红素无法及时排出。研究显示,母乳摄入量不足的新生儿黄疸发生率比充分喂养者高2.5倍。
2. 遗传代谢缺陷:G6PD缺乏症、Gilbert综合征等遗传病会干扰胆红素代谢,这类患儿黄疸可能持续至出生后3周以上。
三、黄疸的临床分型与识别要点
(一)生理性黄疸
(二)病理性黄疸
四、分级诊疗策略与家庭护理
(一)医疗干预
1. 光疗:蓝光(波长425-475 nm)可将未结合胆红素转化为水溶性异构体,适用于TSB>15 mg/dL的患儿。新型光纤毯技术可实现家庭光疗,减少母婴分离。
2. 换血疗法:当TSB>25 mg/dL或出现神经系统症状时,需紧急换血清除游离胆红素。
(二)家庭管理
1. 喂养技巧:母乳喂养者每天至少8-12次,配方奶喂养按需供给。添加益生菌(如双歧杆菌)可加速胆红素排泄。
2. 观察记录:使用手机APP(如BiliScan)每日拍摄婴儿面部、胸部皮肤,AI算法可初步评估黄疸程度。
五、预防策略与未来方向
1. 产前筛查:对O型或Rh阴性血孕妇进行抗体筛查,必要时孕晚期注射免疫球蛋白。
2. 技术创新:经皮胆红素仪(TcB)联合Kramer法则评估法,可减少70%的血液检测需求。
3. 基因检测:针对有黄疸家族史的夫妇,建议进行G6PD、UGT1A1基因检测。
新生儿黄疸的管理需科学性与人文关怀并重。家长既要警惕病理性黄疸的警示信号,也不必对生理性黄疸过度焦虑。随着光疗设备家庭化、检测技术无创化的发展,新生儿黄疸的诊疗正朝着更精准、更便捷的方向迈进。当发现婴儿黄疸加重或伴随异常行为时,请立即联系儿科医生——及时的干预是预防严重并发症的关键。
