自闭症谱系障碍(ASD)是一种复杂的神经发育疾病,其核心特征包括社交互动障碍、语言沟通困难以及重复刻板的行为模式。尽管自闭症的确切成因尚未完全明确,但科学研究已揭示其背后涉及遗传与环境因素的复杂交互作用。这种交互不仅塑造了个体的神经发育轨迹,也影响着症状的严重程度和表现形式。理解这种机制,不仅有助于消除公众对自闭症的误解,更能为早期干预和家庭支持提供科学依据。
一、遗传因素:自闭症的“先天密码”
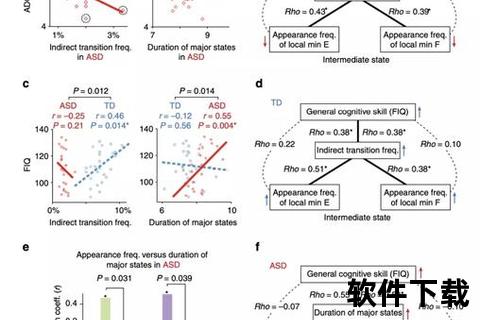
遗传因素是自闭症发病的核心驱动力。研究表明,约80%的自闭症病例与遗传相关,而某些特殊情况下(如染色体16p11.2微缺失),遗传贡献率甚至高达93%。但与传统单基因疾病不同,自闭症的遗传模式具有以下特点:
1. 多基因协同作用:目前已发现超过200个基因与自闭症相关,这些基因涉及神经突触形成、细胞信号传递和表观遗传调控等关键过程。例如,SHANK3基因突变会直接破坏神经元间的连接,而PTEN基因异常则可能导致脑体积异常增大。
2. 随机性与复杂性:即使是同卵双胞胎,自闭症的同病率也仅为60%-90%,这表明除遗传外,其他因素(如孕期环境或基因表达的随机波动)也在起作用。
3. 父母年龄的影响:父亲高龄(≥40岁)会增加子代的自闭症风险,这可能与中积累的基因突变有关;而母亲高龄则与孕期并发症(如妊娠糖尿病)导致的宫内环境变化相关。
值得注意的是,自闭症并非简单的“父母遗传病”。研究显示,多数自闭症患者的基因变异属于新生突变(de novo mutations),即父母并未携带致病基因,而是生殖细胞形成过程中随机产生的。将自闭症归咎于某一方父母的观念并不科学。
二、环境因素:触发风险的“后天钥匙”
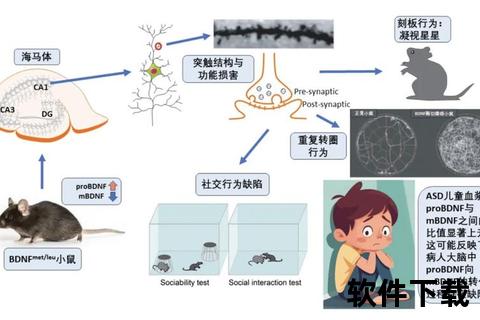
环境因素并非独立致病,而是通过改变基因表达或加剧遗传易感性来影响自闭症的发生。根据暴露时间,环境风险可分为三类:
1. 孕期暴露
2. 围产期损伤
早产、缺氧或产伤可能导致脑部微结构异常。例如,早产儿因未成熟的脑血管易受氧化应激损伤,其ASD风险是足月儿的1.7倍。
3. 早期生活环境
值得注意的是,某些曾被广泛讨论的环境因素(如疫苗中的硫柳汞)已被大规模研究证实与自闭症无关,而城市化带来的噪声污染或电磁辐射仍需更多证据支持其风险。
三、基因与环境的交互机制:从分子到行为的链条
遗传与环境并非独立作用,而是通过以下机制共同塑造自闭症表型:
1. 表观遗传修饰
环境压力(如毒素或营养不良)可改变DNA甲基化或组蛋白乙酰化模式,从而沉默或激活特定基因。例如,孕期叶酸缺乏可能导致MTHFR基因甲基化异常,影响神经管闭合。
2. 代谢通路紊乱
某些基因突变(如线粒体功能相关基因)会使个体对环境中重金属(如汞)的解毒能力下降,导致神经炎症和氧化应激。
3. 神经可塑性受损
环境刺激(如早期社交剥夺)与基因变异(如FMR1基因缺失)协同作用,可能抑制突触修剪过程,导致大脑过度连接和感觉过敏。
一项突破性动物实验显示,给携带自闭症基因的小鼠注射苏拉明(一种阻断细胞应激反应的药物),可逆转其社交障碍和重复行为。这提示未来干预可能通过靶向基因-环境交互节点实现。
四、行动建议:从科学认知到实践
1. 预防策略
2. 早期识别
婴幼儿若出现以下“红色标志”,需尽快评估:
3. 干预原则
4. 社会支持
推动学校融合教育,建立社区康复中心,并通过立法保障自闭症患者的就业权益。
自闭症的成因如同一幅拼图,遗传因素提供了基础框架,环境因素则填充了细节色彩。尽管目前尚无根治方法,但早期干预和系统支持已能显著改善患者的生活质量。对于公众而言,消除“父母教养不当”等偏见,建立包容的社会环境,或许比寻找单一病因更具现实意义。未来的研究需继续探索基因-环境交互的分子靶点,为个性化干预开辟新路径。
